Tendrá fines gineco-obstétricos y solo podrá utilizarse en los hospitales. Hasta ahora, solo estaba aprobado para fines gástricos. Se trata de la droga recomendada por la OMS para interrumpir el embarazo de manera segura.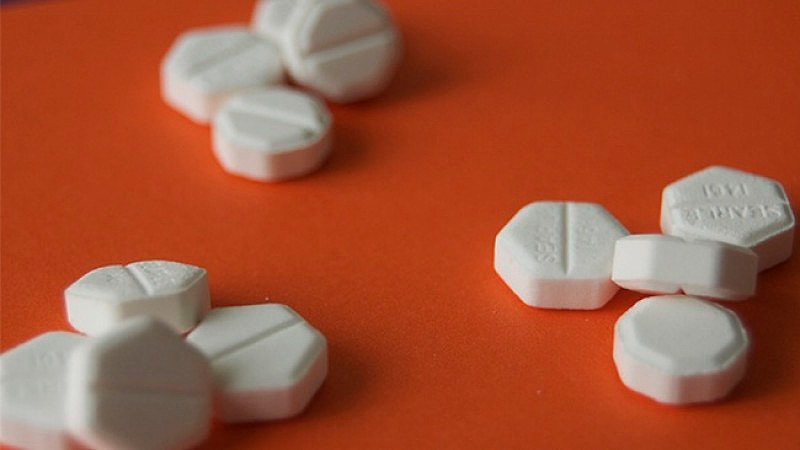
La Autoridad Nacional de Medicamentos, Alimentos y Tecnología (ANMAT) autorizó a un laboratorio nacional a producir misoprostol, la droga que la Organización Mundial de la Salud (OMS) recomienda para abortar de manera segura. Tendrá fines gineco-obstétricos, aunque solo para uso hospitalario.
La medida es del 2 de julio, pero se conoció luego de que el Senado rechazara la semana pasada la legalización del aborto. La producción se realizará en el Laboratorio Domínguez. Y su directora técnica, la farmacéutica Sandra Rismondo, calcula que antes de fin de año podrán producir el medicamento y que se presentarán en las licitaciones que realice el Ministerio de Salud para la compra de la droga.
En la disposición 6726/2018 del 2 de julio, la ANMAT estableció: «Autorízase a la firma Laboratorio Dominguez S.A. para la especialidad medicinal que se denominará MISOP 200, la nueva concentración de Misoprostol 200 mg, forma farmacéutica comprimidos vaginales».
Asimismo, en el anexo de la autorización, la agencia permitió la comercialización de envases con 4, 8, 20, 48 y 100 comprimidos, con la condición de venta exclusiva con receta archivada y para uso hospitalario.
Hasta ahora, lo único que podía conseguirse en las farmacias era el medicamento llamado Oxaprost, una presentación que se combina con diclofenac y que sólo está permitida para uso gástrico, no para fines ginecológicos, como ahora sí autoriza la ANMAT al misoprostol.
Lo que le solicitó la ANMAT al laboratorio fue la presentación de un Programa de Gestión de Riesgo como condición para la aprobación del producto. Está basado en tres claves: «1) La venta se realiza exclusivamente a instituciones hospitalarias que cuentan con servicio de obstetricia. 2) Los hospitales completan formularios especiales para la compra del medicamento, informando sobre el uso del producto medicinal y el número promedio de partos en la institución. 3) El laboratorio titular informa a ANMAT los movimientos del producto y los datos recopilados en los formularios de compra del medicamento».
Rismondo contó también que pidieron un cambio en las condiciones de expendio para poder venderlo en farmacias directamente al público, siempre bajo receta archivada. Actualmente, la ANMAT se encuentra evaluando ese requerimiento.






